Marcatura CE Apparecchiature Radio – RED
La direttiva 2014/53/UE richiede la marcatura CE obbligatoria su tutte le apparecchiature di radio trasmissione.
Introduzione alla marcatura CE delle apparecchiature radio
La marcatura CE delle apparecchiature radio (RED) è una procedura obbligatoria per tutti i prodotti disciplinati dall’omonima direttiva comunitaria. Deve essere eseguita dal fabbricante, se residente sul territorio UE o da un suo mandatario, purché Europeo, il quale dichiara per mezzo della dichiarazione di conformità, che il suo prodotto è conforme ai requisiti di sicurezza e salute, previsti dalle direttive pertinenti.
La nostra società fornisce l’assistenza e la consulenza necessarie per la marcatura CE dei dispositivi di radio trasmissione ed il servizio di gestione del fascicolo tecnico.
Forniamo inoltre il servizio di estensione del fascicolo tecnico a tutte le apparecchiature radio del Vostro catalogo
Approfondimento marcatura CE apparecchiature radio
Esiste una direttiva che si occupa della limitazione delle onde elettromagnetiche, in quanto possono essere fonte di disturbo.
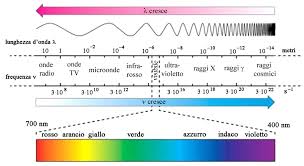
Quelle stesse onde che sono presenti ovunque nel nostro mondo, la stessa luce è formata da onde elettromagnetiche, sono utilizzate per le trasmissioni radio e video.
Quando le apparecchiature utilizzano le onde elettromagnetiche per il loro funzionamento, devono rispettare la direttiva 2014/53/UE “Dispositivi radio”. La definizione ufficiale di «apparecchiatura radio» è: “un prodotto elettrico o elettronico che emette e/o riceve intenzionalmente onde radio a fini di radiocomunicazione e/o radiodeterminazione o un prodotto elettrico o elettronico che deve essere completato con un accessorio, come un’antenna, per poter emettere e/o ricevere intenzionalmente onde radio a fini di radiocomunicazione e/o radiodeterminazione;”
La direttiva impone l’obbligo di marcatura CE dei dispositivi radio.
Quali sono i prodotti radio più comuni? Certamente il prodotto più diffuso tra i dispositivi di radio trasmissione è il telefono cellulare e lo smartphone, ma ce ne sono molti altri che utilizziamo ogni giorno, come ad esempio tutti i dispositivi Bluetooth e quelli wireless.
Gli apparecchi di radio trasmissione devono rispettare per gli aspetti di sicurezza sia la direttiva 2014/35/UE Bassa tensione, sia la direttiva 2015/30/UE Compatibilità elettromagnetica e devono avere dei certificati o documenti che ne dimostrano il rispetto dei range di funzionamento (in base alle norme armonizzate), a meno che il loro raggio di azione non sia molto limitato.
I certificati di prova o altri documenti rilasciati da Organismo Notificato e non, NON sostituiscono comunque la marcatura CE, ma la integrano.
Un produttore extra europeo NON può fare la marcatura CE delle apparecchiature radio. Se lo fa è illegale.
Fascicolo tecnico apparecchiature radio
Ogni dispositivo radio deve essere completamente definito dal punto di vista della sicurezza, da un fascicolo tecnico che è composto da:
-
-
- analisi dei rischi
- manuale di installazione, d’uso e di manutenzione
- dichiarazione di conformità
- etichetta CE
- progetti, disegni, relazioni di calcolo, schemi, foto e quant’altro possa illustrare in modo completo la macchina ed i suoi componenti
- distinta base componenti
- elenco dei fornitori
- procedure di controllo della produzione
-
Ti interessa parlarne? Fatti richiamare.
Lascia i tuoi dati e sarai richiamato senza impegno.
Ascolta il podcast
La conformità dei dispositivi radio - Domande e risposte
Regolamenti e direttive
Puoi consultare la direttiva cliccando sul link seguente: Direttiva apparecchiature Radio RED 2014/53/UE (link UE)
Referenze
Possiamo farTi superare le difficoltà di un argomento complesso, con efficacia ed efficienza.
Prima di Te hanno lavorato con noi:
-
-
- centinaia di aziende, proprio come la Tua
- multinazionali che operano in vari settori produttivi, dal petrolifero all’oleodinamico
- Guardia di Finanza
- Polizia Tributaria
- Carabinieri
- Polizia di Stato
- Dogane e spedizionieri
-
Consulta le nostre referenze per vedere con chi abbiamo lavorato.