Marcatura CE delle mascherine protettive
Il Coronavirus colpisce basso: scopriamo assieme tutto quello che serve sapere sulla marcatura CE di questo dispositivo medico.
Marcatura CE delle mascherine protettive
Che la loro destinazione d’uso sia come dispositivo medico o DPI, la marcatura CE delle mascherine protettive è obbligatoria.
Dispositivi medici o DPI, le mascherine protettive necessitano sempre di marcatura CE
Il coronavirus sta producendo anche fenomeni economici sui quali è opportuno riflettere.
La domanda di mascherine protettive è salita enormemente e la sollecitudine di molti imprenditori, verso le necessità delle persone a rischio ha fatto sì che anche aziende non di questo settore, si mettessero subito all’opera.
Questo comporta la necessità di chiedere informazioni e di cercare di capire in primis cosa sono queste mascherine e se hanno bisogno di marcatura CE.
Innanzitutto, precisiamo che si prestano a due diverse tipologie di utilizzo:
- come dispositivi medici;
- come dispositivi di protezione individuale.
Quando le mascherine sono dispositivi medici
Quando considerate dispositivi medici, le mascherine protettive necessitano di marcatura CE in quanto barriere meccaniche protettive. Rientrano nella classe di rischio I e devono essere registrate al Ministero della Salute.
Per mantenere un profilo basso (“meglio evitare la registrazione al Ministero”) e perché indirizzati da chi produce certificati di qualsiasi tipo, alcuni le vogliono considerare dispositivi di protezione individuale, che certamente non sono utilizzati dai comuni cittadini.
Approfondiamo quindi una questione che conoscevamo da anni, ma che abbiamo sempre lasciato perdere, per non sollevare vespai. Ci vengono richieste spiegazioni e consulenza sulle mascherine FFP1 o altro, quindi forniamo un chiarimento.
Quando le mascherine sono DPI
Quando considerate DPI, le mascherine protettive hanno l’obbligo di marcatura CE come tali. Il Regolamento (UE) 2016/425 sui dispositivi di protezione individuale (link al sito ufficiale), così come la precedente direttiva, suddivide i DPI in 3 categorie: I, II, III e nulla hanno a che fare con le classi di protezione FFP1, FFP2, FFP3.
Le categorie sono ben definite nell’allegato I del Regolamento che definisce, senza distinzione di categoria III, i DPI che proteggono da:
- a) sostanze e miscele pericolose per la salute;
- b) atmosfere con carenza di ossigeno;
- c) agenti biologici nocivi.
Inoltre, nella categoria I, non si trova segno di alcuna protezione delle vie respiratorie, quindi TUTTE le mascherine rientrano nelle categorie II o III. Queste a loro volta potranno essere suddivise in diverse classi di protezione.
Confondere la classe di protezione con la categoria è un errore.
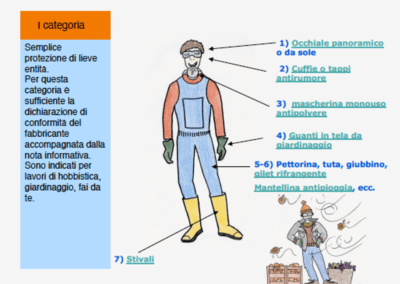
In esso è incorso anche l’estensore di questo volantino, di cui forniamo stralci e peraltro patrocinato da eminenti autorità:
Attenzione:
Il “fabbricante”, cioè non necessariamente il produttore, ma chi rende disponibile un prodotto sul mercato UE, deve costituire l’intero fascicolo tecnico nel rispetto delle leggi.
In base a che criterio effettuare la marcatura CE delle mascherine protettive?
Le mascherine che proteggono dalla polvere, quelle leggere acquistabili ovunque, non sono di categoria I. La categoria minima è la II. Per essere marcate hanno necessità di un test e/o altro tipo di intervento anche da parte di un Organismo Notificato, cosa che non compare mai nella loro marcatura CE.
In sostanza, come dispositivi medici si possono immettere in commercio senza particolari problemi e verifiche, perché rappresentano una barriera meccanica contro possibili agenti nocivi.
Come DPI invece devono superare dei test che, incomprensibilmente, in alcuni ambiti si eseguono sempre e spesso a sproposito mentre in questo particolare settore della sicurezza non sono ritenuti necessari, quando invece la legge li prevede.
Ovviamente, se gli errori sono avvallati da chi deve sorvegliare la sicurezza sui luoghi di lavoro, si può giustificare, forse, chi inconsapevolmente o meno, sceglie la strada più facile e commercializza questi DPI in contrasto con le leggi europee.
Ascolta il podcast
Dispositivi medici - Domande e risposte
I nostri videotutorial su…
Regolamenti e direttive
I dispositivi medici devono essere marcati CE, applicando le procedure che sono indicate in questo sito e sulle quali la nostra società fornisce assistenza e consulenza.
Puoi consultare i regolamenti e le direttive cliccando sui seguenti link:






Buongiorno, nel caso in cui un produttore sia autorizzato in deroga dall’ISS per la produzione di mascherine chirurgiche ed abbia marcato CE le mascherine, può esportare le suddette mascherine all’estero? E’ sufficiente questa documentazione o è necessaria comunque la certificazione di un organismo notificato?
Grazie mille
Salve, un prodotto marcato CE può essere venduto liberamente in tutta UE, sulla deroga ISS preferisco non rispondere, TUTTI, ma proprio TUTTI, anche quelli che hannon seguito tale pratica, sanno benissimo di cosa si tratta.
Cordiali saluti
Ing. Carraro
Buongiorno,
se una società produce mascherine ad uso medico dotate di marcatura CE e autorizzate in deroga dall’ISS, può esportarle all’estero o è necessaria la certificazione presso un organismo notificato?
Ho capito che può esportarle in quanto marcate CE dal fabbricante, ma possono essere esportate come “certificate” con la sola autorizzazione dell’ISS?
Grazie mille
L’autorizzazione ISS non ha nulla a che vedere con le leggi europee e con il buon senso, tragga lei le conclusioni.
Cordiali saluti
Ing. Carraro
Salve, se inquadriamo la mascherina chirurgica come dispositivo medico posso marcare CE il mio prodotto rilasciando la dichiarazione di conformità in autodichiarazione come da Allegato VII della direttiva 93/42 CE? Da questo momento in poi posso commercializzarlo in tutta Europa?
In questo caso, a cosa serve la registrazione presso il Ministero della Salute?
Grazie
Salve, innanzitutto non si tratta di inquadrare, ma di stabilire se un prodotto è dispositivo medico, che ha quindi l’obbligo della marcatura CE in base alla pertinenti direttiva, dopodiché si prepara il fascicolo tecnico all’interno del quale c’è tra gli altri documenti la dichiarazione di conformità, che è SOLO una componente del fascicolo tecnico e non è sostituiva della marcatura CE.
Il dispositivo può essere venduto in tutta l’UE, ma in alcuni Paesi è necessaria anche la registrazione al Ministero delle Salute, perchè lo prevede una legge di quello Stato.
In futuro la registrazione sarà a livello europeo, sarà unica e si chiamerà codice UDI, questo dimostra che l’esempio italiano era corretto ed è stato seguito da tutta L’UE.
Cordiali saluti
Ing. Carraro
Buongiorno, devo importare delle
mascherine generiche dal giappone
e venderle nel mercato italiano.
le scatole non hanno marchiatura ce..
oltre alla dichiarazione di conformità del produttore
che dichiara….ecc…
con mandante europeo..quali documenti ancora presentare?
avete un modulo precompilato (inglese) da dare al produttore cinese?
grazie
Salve, in ogni caso lei deve predisporre un fascicolo tecnico, per le generiche non c’è obbligo e possibilità di marcatura CE.
Cordiali saluti
Ing. Carraro
non escodalla mia abitazione da oltre un mese, ho 80 anni, e mi sapreste indicare dove acquistare mascherine idonee al coronavirus. Grazie
Salve se vuole sono in vendita nel nostro sito e le spediamo senza che Lei si sposti da casa.
Cordiali saluti
Ing. Carraro