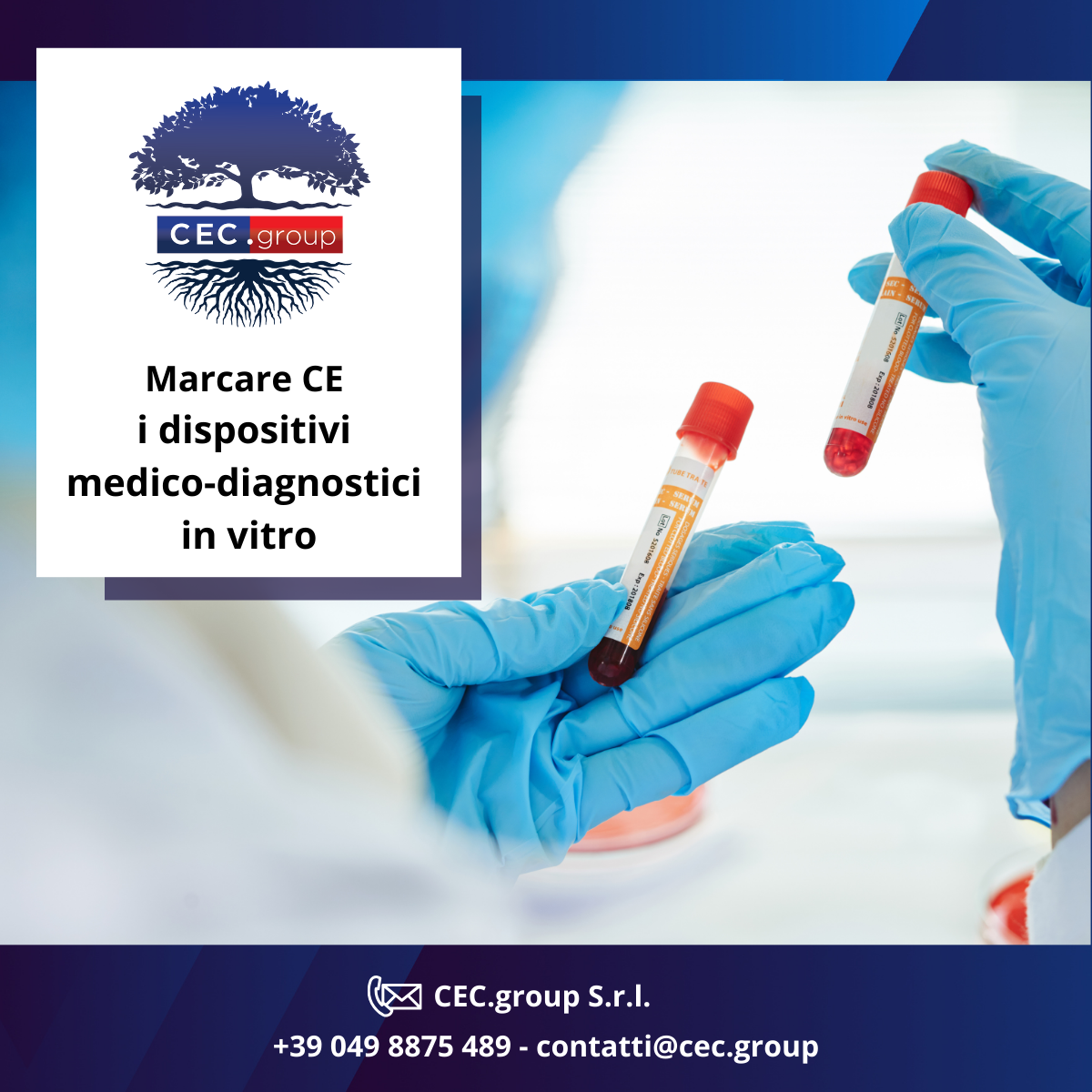
Marcare CE i dispositivi medico-diagnostici in vitro (IVD)
I dispositivi medici di diagnosi in vitro sono prevalentemente utilizzati da personale sanitario, solo alcune tipologie sono a disposizione dei pazienti.
Marcare CE i dispositivi medico-diagnostici in vitro è un obbligo in quanto questi prodotti sono disciplinati dal Regolamento (UE) 2017/746.
Cosa sono i dispositivi medico-diagnostici in vitro?
Sono dei dispostivi che consentono di fornire una risposta diagnostica rispetto ad una ricerca specifica. In sostanza sono dei prodotti che consentono di portare a termine dei test.

Chi sono gli utilizzatori del dispostivi di diagnosi in vitro?
I dispositivi di diagnosi in vitro sono utilizzati per lo più da operatori sanitari in quanto sono necessari per tutti gli esami di laboratorio, alcuni tipi destinati ad attività più semplici sono utilizzabili anche dai pazienti direttamente, ad esempio alcuni contenitori per il prelievo di sostanze organiche sono a disposizione di tutti i cittadini.
Attenzione
I dispositivi di diagnosi in vitro sono divisi per tipologia e solo la più semplice è utilizzabile dai cittadini/pazienti. Le altre tipologie contengono o sono in genere sostanze, che partecipano alle reazioni chimiche che consentono di rilevare specifiche patologie.
La disponibilità di dispositivi di diagnosi in vitro di categoria superiore alla prima non avrebbe alcun senso per il cittadino comune in quanto essi non sono utilizzabili senza specifici supporti ed apparecchiature.
Un esempio di dispositivo di diagnosi di utilizzo comune?
Il test di gravidanza è certamente un dispositivo di diagnosi molto diffuso ed utilizzato dalle donne di tutto il mondo ormai da anni. Un altro tipo, purtroppo ben noto ed ancora attuale, è quello del test covid.
Nota bene
I tempi e le modalità di marcatura CE sono definite da una legge che sta al di sopra di tutte le altre e stabilisce chi, come e quando deve fare la marcatura CE. Ecco cosa dice il Regolamento Macchine: La marcatura CE è soggetta ai principi generali esposti del Regolamento (CE) n. 765/2008. Quindi non è più il singolo regolamento o la singola direttiva ad indicare come fare la marcatura CE, ma il Regolamento (CE) n. 765/2008.
Finalmente le leggi cominciano ad essere interconnesse invece di andare ognuno per proprio conto.
Quali sono gli obblighi del fabbricante di dispositivi medico-diagnostici in vitro?
Il fabbricante, cioè colui che immette sul mercato i dispositivi di diagnosi in vitro, deve predisporre tutta la documentazione tecnica (fascicolo tecnico) che dimostri che il dispositivo rispetta il Regolamento (UE) 2017/746 e le eventuali norme specifiche ad esso armonizzate. Per i dispositivi di diagnosi in vitro di categoria superiore alla prima, deve rivolgersi ad un organismo notificato che rilascia un certificato di conformità in base a test e verifiche eseguite su un campione di prodotto.
Cosa deve controllare chi utilizza un dispositivo di diagnosi in vitro, sia destinato ad uso professionale, che privato?
Il controllo deve riguardare la presenza del marchio CE ed eventualmente delle quattro cifre che identificano l’organismo notificato eventualmente intervenuto nel processo di marcatura CE. Devono inoltre essere disponibili le istruzioni d’uso (bugiardino) e la dichiarazione di conformità. Sul prodotto deve essere presente il codice a barre che lo identifica in modo univoco.
Hai bisogno di informazioni su come marcare CE i dispositivi medico-diagnostici in vitro?
Noi di CEC.group possiamo assisterti in tutto il percorso obbligatorio per immettere i tuoi prodotti legalmente nel Mercato Europeo nel rispetto del diritto comunitario.
Sei un produttore, un importatore, un mandatario? Ti guidiamo attraverso la marcatura CE e la conformità dei prodotti.
Contattaci per ottenere maggiori informazioni ed eventuale consulenza, Ti risponderemo velocemente ed in ogni caso. Clicca qui!
Devi fare la marcatura CE di dispositivi medico-diagnostici in vitro?
Inserisci il tuo recapito e sarai contattato.
Leggi altre informazioni, ascolta i podcast, guarda i video
- Marcatura CE dispositivi medici, cosa serve e come fare
- Marcare CE i dispositivi medici invasivi
- Novità sulla registrazione EUDAMED
Inoltre:
Dispositivi medici - Domande e risposte
Fabbricante, produttore, mandatario, importatore – Che ruoli hanno questi soggetti in relazione alla marcatura CE?
Referenze
Possiamo farTi superare le difficoltà di un argomento complesso, con efficacia ed efficienza.
Prima di Te hanno lavorato con noi:
-
-
- centinaia di aziende, proprio come la Tua
- multinazionali che operano in vari settori produttivi, dal petrolifero all’oleodinamico
- Guardia di Finanza
- Polizia Tributaria
- Carabinieri
- Polizia di Stato
- Dogane e spedizionieri
-
Consulta le nostre referenze per vedere con chi abbiamo lavorato.